Otitis Externa Maligna – Morelli Sebastián – 2006
Objetivos
La otitis externa maligna es una infección que involucra al hueso temporal y tejidos adyacentes, siendo una complicación relativamente rara de una otitis externa.
Ocurre principalmente en personas con inmunodeficiencias, diabéticas (en especial insulinodependientes), añosas, trauma iatrogénicos del canal auditivo externo, ateroesclerosis, corticoideoterapia, etc.
El patógeno mas frecuentemente involucrado es Pseudomona aeruginosa.
Clásicamente se presenta con granulaciones en el CAE, especialmente en la unión de cartílago con hueso, cuando compromete nervio facial y otros pares craneales, indica peor pronostico, siendo las complicaciones endocraneanas las causas de muerte.
El diagnostico requiere una adecuada anamnesis, cultivo de las secreciones oticas y examinacion de las granulaciones.
Los estudios por imágenes incluyen TAC, Tc 99, Ga 67.
El tratamiento consiste en corregir dentro de lo posible el estado de inmunosupresion, controlar la diabetes, tratamiento local del CAE, ATB sistémicos, y en algunos pacientes, cirugía.
Las personas con riesgo de esta complicación, deben ser educados en la manipulación del CAE (evitar cotones y lavajes) y minimizar el contacto con agua en los oídos.
En este monografía se hará enfoque en el seguimiento de esta patología con los estudios antes mencionados, recalcando criterios de curación, seguimiento y pronostico, haciendo especial hincapié en su tratamiento, mencionando el uso de cámara hiperbárica y sus efectos sobre esta patología, sin dejar de rermarcar sus contraindicaciones.
También considero de vital importancia, nombrar los estudios por imágenes que se disponen en la actualidad, no solo para diagnostico, sino para pronostico, evaluación y curación de esta patología, esencialmente centellografìa.
También se hará revisión sobre entidades etiológicas, factores predisponentes y signo sintomatología.
Introducción
La OEM fue relatada hace ya más de cien años (1881) por Raymond, quien la observó en pacientes diabéticos.
El primer caso de otitis externa maligna fue descripto por Meltzer y Keleman en 1959 y en 1968 Chandler fue quien describió una serie de trece pacientes, principalmente diabéticos afectados por procesos inflamatorios necróticos en el conducto auditivo externo, causado por Pseudomona aeruginosa, con complicaciones frecuentes en la base del cráneo). Son sinónimos de esta enfermedad, utilizados en diferentes países, otitis maligna del diabético, osteomielitis de base de cráneo, otitis externa necrotizante.
La OEM es ocasionada casi exclusivamente por Pseudomona aeruginosa, bacilo gram negativo, que se aísla en el suelo, agua, plantas y animales, incluyendo a los seres humanos. Es ocasionalmente patógeno para las plantas y animales. Raramente causa enfermedad en las personas saludables, aunque es un saprofito humano muy común.
La infección se origina generalmente en el conducto auditivo externo (CAE), sobrepasa su revestimiento cutáneo, progresa y da lugar a una condritis y/o osteomielitis. La infección pasa a través de la incisura de Santorini (que es un pequeño surco situado en el piso del CAE cartilaginoso, el cual esta relleno de tejido conectivo, nervios y vasos sanguíneos) y de la unión de la porción cartilaginosa y ósea del CAE, posteriormente se desarrolla un tejido de granulación que se extiende por las cavidades del peñasco y base del cráneo. La infección también puede progresar a través del tímpano, penetrar en las cavidades aireadas del hueso temporal, el peñasco, las estructuras anatómicas vecinas, e incluso, el tallo cerebral.
Aparece en pacientes con alteraciones del sistema inmunológico, sobre todo diabéticos (90 %), en general insulinodependientes y mal controlados, aunque la OEM no coincide necesariamente con un periodo de hiperglucemia, pacientes añosos, bajo quimioterapia, leucemias, corticoideoterapia, ateroesclerosis, hipogamaglobulinemias, etc.
Es mas frecuente en hombres, con variaciones en los diferentes reportes que van de 1,8 a 1 a 18 a 1, presentándose excepcionalmente en niños. Es de destacar, que la infección se produce por la combinación de un germen agresivo y un terreno debilitado.
A continuación, se describirán algunas de los trastornos propias del paciente diabético:
• La Infección es una de las complicaciones más frecuentes en la diabetes.
• La tasa de mortalidad por infecciones en los pacientes diabético es importante.
• La diabetes predispone a la adquisición de Infecciones.
• Las infecciones dificultan el control de la diabetes.
• Existe la posibilidad de inducción de la diabetes a partir de infecciones virales.
• Alteración de la flora microbiológica normal con aumento de colonización por estafilococos, anaerobios y levaduras
• Alteración de los polimorfonucleares
– La hiperglucemia altera la función fagocítica.
– Disminución de la quimiotaxis.
– Déficit leucocitario: disminución de fagocitosis y déficit de inactivación.
• Alteración linfocitaria: falla de inmunidad celular.
• Disminución en la liberación de linfocitos, complemento y anticuerpos en el área de infección.
• Los tejidos necróticos e isquémicos se pueden transformar en focos infecciosos
• Frecuencia aumentada de infecciones polimicrobianas.
• Tendencia a la necrosis tisular, con formación de gas en los tejidos.
• Mayor incidencia de Bacteriemias y complicaciones viscerales.
Por otra parte, P.aeruginosa tiene afinidad especial por los vasos (angeitis necrotizante), libera toxinas y enzimas proteolíticas que induce necrosis titulares, activación de la cascada inflamatoria y presentando además, resistencia a la fagocitosis.
Actualmente se encuentran muchas dificultadas en la interpretación de éstos cuadros, particularmente en las formas menos severas de OEM sin complicaciones, donde hacer un diagnóstico diferencial con las otitis externas no malignas, no es siempre fácil de hacer.
Antes del uso de antibióticos como las penicilinas y los aminoglucósidos; la base del tratamiento fue la cirugía radical. De cualquier modo la tasa de mortalidad mejoró progresivamente con la rápida y temprana administración de antibióticos antipseudomona y una limpieza conservadora de los granulomas tisulares y óseos.
Etiología
P. Aeruginosa puede ser cultivada en el 96 a 98% de los casos de OEM. Raramente causa infección en tejidos perfectamente sanos, pero generalmente progresa desde una pequeña lesión continua, recientemente se ha hallado que en más del 50% de los casos de OEM es precedida por maniobras en el CAE.
Aspergillus fumigatus: Es rara la OEM causada por la infección de un hongo .Se ha informado acerca de un extraño caso de OEM causada por Malassezia Sympodialis en un hombre de 53 años diabético no insulinodependiente.
S. epidermidis: Este germen es habitualmente un microorganismo no patógeno, sin embargo, han sido reportados casos ocasionados por el mismo, el cual fue aislado en casi todos los cultivos de oídos de estos pacientes con OEM, pero casi nunca era reconocido como el agente patógeno.
Clínica
La OEM presenta rasgos clínicos que raramente permiten hacer un diagnóstico precoz exacto. Los signos y síntomas al comienzo son inespecíficos y es difícil distinguirlo de una otitis externa benigna. Esto explica porqué el diagnostico es generalmente tardío. Los pacientes presentan otalgia en mas del 90 % de los casos, siendo el síntoma inicial mas común.
La otorrea, generalmente fétida, se asocia al dolor en el 45 a 100 % de los casos. Usualmente se halla Hipoacusia conductiva leve. La fiebre es de rara aparición. La sintomatología vascular y de pares craneales se halla en estadios mas avanzados de la patología
A continuación se presenta un cuadro con porcentajes de la sintomatología más común que acompaña dicha enfermedad:
|
Variables Clínicas Cuantitativas
|
Diabetes Tipo 1 (n=4)
|
Diabetes Tipo 2 (n=18)
|
||
|
Media
|
DE
|
Media
|
DE
|
|
|
Edad (años)
|
47,2
|
14,9
|
70,8
|
9,8
|
|
Edad de la presentación de la DM (años)
|
20,2
|
5,1
|
47,6
|
6,5
|
|
Evolución de la DM (años)
|
22,5
|
10,0
|
27,5
|
11,7
|
|
Glucemia (mmol/L)
|
11,4
|
2,9
|
8,8
|
3,3
|
|
Estadía Hospitalaria (días)
|
16,5
|
9,0
|
55,3
|
3,3
|
|
Sexo (M/F)
|
3/1
|
8/10
|
||
|
Tratamiento de la DM (No. /%) Compuestos Orales Hipoglucemiantes
|
–
|
11 (61,1%)
|
||
|
Compuestos Orales Hipoglucemiantes + Insulina de acción Intermedia
|
–
|
1 (5,6%)
|
||
Signos clínicos
Casi siempre existe la presencia de tejido de granulación en el CAE, generalmente a nivel de la unión osteocartilaginosa del piso del CAE, o de la pared anterior del conducto.
El CAE suele estar edematoso y estenótico debido al edema y a la sumatoria de los granulomas.
La membrana timpánica no se logra visualizar y cuando eso es posible, es generalmente de aspecto normal, aunque puede existir secreción serosa
La palpación puede revelar un edema blando por debajo del CAE entre la mastoides y la rama ascendente del maxilar inferior; pudiéndose ver en estadios posteriores mala función, dolor o alteraciones en la sensibilidad de la articulación temporomandibular.
Los hallazgos de laboratorio suelen ser generalmente inespecíficos. Es muy frecuente encontrar en estos pacientes una hiperglucemia y una disminución de la tolerancia a la glucosa, acompañada casi siempre por un aumento en la velocidad de eritrosedimentación, este último es al hallazgo mas frecuente.
La biopsia informa tejido con ulceración y granulaciones, con proceso inflamatorio agudo o crónico
Fotografia de paciente con OEM
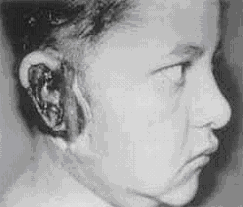
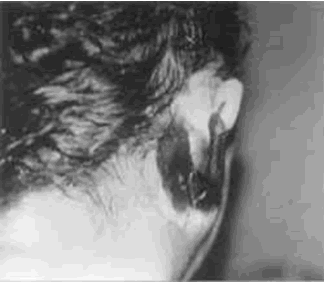
Evolución
Presenta una mortalidad elevada, de 20 % cuando no existe afectación de pares craneales, trepando al 50 % si presenta parálisis facial y 60 al 80 % cuando otros pares craneales están afectados.
Las recidivas son posibles y las parálisis de los nervios craneales suelen ser definitivas.
Su evolución es siempre la misma, comienza con efracción del CAE poco importante (extracción de cerumen, baños en piscina, uso de hisopos) que conduce a una celulitis dolorosa.
Esta celulitis, se acompaña de otorrea en el 50 al 80 % de los casos, otalgia intensa (75 % de los casos presente) y cefaleas intensas.
El punto de partida es una lesión de la piel del conducto auditivo externo por un traumatismo local poco importante (a menudo después de un lavado de oído, de un baño en una piscina) que provoca una celulitis dolorosa en el conducto auditivo externo, acompañada de otorrea, edema, estenosis y un pequeño granuloma en el piso del CAE.
La infección puede tomar diferentes caminos.
Hacia anterior, erosionando la pared anterior del CAE, comprometiendo la articulación temporomandibular.
Hacia inferior, siguiendo la fisura de Santorini, invade los tejidos blandos de la fosa infratemporal, el espacio parotídeo, el espacio de los músculos masticadores (produciendo una parotiditis circunscripta primero y luego difusa, con presencia de trismus por irritación del músculo masetero), y la parte alta del espacio o vaina carotídea. Desde aquí el proceso inflamatorio puede llegar al agujero estilomastoideo o por igual al foramen yugular. Hacia posterior, puede destruir el hueso cortical de la apófisis mastoides e invadir las cavidades neumatizadas , lo cual es menos común. Desde las mastoides y a través del antro y del aditus puede extenderse al oído medio, y a la punta del peñasco, al laberinto, etc.
En general el oído medio se afecta por vía retrógrada (antro-atical), y en forma tardía. Externamente, comprometiendo el pabellón de la oreja y los tejidos blandos vecinos, con condritis del conducto auditivo externo.
Internamente, invadiendo el peñasco y desde allí el laberinto. Finalmente la infección puede también propagarse a lo largo de los canales vasculares (seno lateral, seno petroso superior e inferior) y la superficie ósea de la pirámide; y desde acá ambas extenderse a la fosa cerebral media y posterior, pudiendo llegar hasta el ápex petroso.
Así de esta forma la infección puede extenderse por al clivus hacia el seno esfenoidal y dirigirse hacia el hueso temporal contralateral. La membrana timpánica, resiste la infección por lo que el oído medio suele ser invadido a través de las cavidades mastoideas. El laberinto es resistente a la infección y su compromiso es siempre tardío. Las zonas de neumatización del hueso temporal y la cápsula ótica, están generalmente respetadas.
Complicaciones
Osteomielitis de La Base del Cráneo. Esta es una complicación natural de la OEM cuando no es tratada adecuadamente y oportunamente. Puede desarrollarse como extensión directa de una infección aun presente en el CAE u otro (en éste caso por un tratamiento inadecuado) y aparecer algún tiempo después que el proceso primario aparentemente ha desaparecido, manifestándose con una cefalea intensa en forma aguda.
Parálisis de los Nervios Craneales. Una progresión más amplia de la osteomielitis hacia el foramen de la base del cráneo puede llevar a ésta complicación. Según algunos autores, las afecciones nerviosas aparecen a menudo después de dos meses de evolución.
En algunas estadísticas esta eventualidad ha sido establecida por encima del 40% de los pacientes.
La parálisis puede ser única o múltiple y en casos avanzados ser bilateral. La progresión del proceso infeccioso se efectúa entonces de afuera hacia adentro, con parálisis sucesivas de los nervios craneanos que emergen de la cara inferior del peñasco en un 30% a 40% de los casos. El nervio mas comúnmente afectado es el facial, el cual se presenta en el 60% de los casos. En general a nivel de su tercera porción o a la salida el agujero estilomastoideo.
Es menos frecuente la complicación a nivel del foramen yugular de los pares craneales IX, X y XI (agujero rasgado posterior), produciendo disfonía, disfagia, aspiración y disnea. Son raros de igual forma el compromiso de los nervios VI y XII.
También se han reportado casos de Neuritis óptica como complicación en procesos de OEM, todos éstos casos presentados permanecieron refractarios al tratamiento estándar, reportándose que solo uno de ellos sobrevivió, pero que fue curado con oxígeno hiperbárico.
Osteomielitis de la Articulación Temporomandibular. En general suele ser una osteomielitis destructiva y el diagnóstico suele hacerse por TC ó RMN.
Otras Complicaciones. En general se dan por extensión del proceso y son complicaciones potencialmente letales. Entre ellas tenemos:
• Meningitis.
• Absceso cerebral.
• Tromboflebitis de la vena yugular interna y del seno lateral.
• Trombosis de la arteria carótida interna.
Diagnostico
El diagnóstico de la OEM es clínico, basándose en el antecedente de una otitis externa progresiva, refractaria al tratamiento usual de una forma benigna, en un paciente inmunosuprimido o diabético de edad avanzada. En una forma invariable, hay tejido de granulación en la zona de unión osteocartilaginosa del CAE observándose en forma ocasional poco cartílago o cartílago necrótico en este sitio; este tejido de granulación debe ser biopsiado para determinar la etiología infecciosa de la misma.
El tímpano por lo general está intacto, el cultivo es positivo para Pseudomona aeruginosa. El severo dolor producido en esta afección permite seguir el progreso del tratamiento. La recurrencia del dolor después del aparente control es un signo ominoso y justifica un manejo agresivo. Si bien el diagnóstico de OEM se hace por medio criterios clínicos, es difícil determinar la extensión de la enfermedad; siendo necesario contar con información adicional en cuanto a la extensión exacta de la infección en los tejidos blandos y el hueso en la base del cráneo.
Existen diferentes criterios clínicos para el diagnóstico de OEM los cuales se han ido modificando con el curso del tiempo según los diferentes autores
Corey (1985):
Por lo menos deben existir tres de estas cinco manifestaciones propuestas:
1. Otitis externa persistente.
2. Tejido de granulación en el CAE.
3. Evidencia de mastoiditis u osteomielitis de la base del cráneo por biopsia o estudios por imágenes.
4. Parálisis de nervios craneales.
5. Aislamiento de Pseudomonas en el CAE.
Según Cohen (1987):
— Signos mayores (obligatorios):
— Dolor.
— Exudado.
— Edema.
— Granulaciones.
— Micro abscesos.
— Centellografìa c/Tc 99 (+) luego de una semana de tratamiento local.
— Pseudomona
Signos menores (ocasionales):
— Pseudomonas.
— Rx (+).
— Diabetes Mellitus.
— Compromiso de nervios craneales.
— Condiciones debilitantes de paciente.
— Edad avanzada.
Babiatzki (1987) – Sade (1989):
o Otitis externa severa que no responde a tratamiento conservador luego de 8 días.
o Dolor, especialmente a la noche.
o Tejido de granulación especialmente en la base del CAE.
o Cultivo (+) para Pseudomona.
o Centellografìa (+) de hueso temporal.
o Diabetes.
Sade (1989):
• Otitis externa severa que no responde a tratamiento conservador luego de 10 días.
• Incremento progresivo del dolor, el cual se exacerba por la noche.
• Tejido de granulación el cual es típico, especialmente en la base del cráneo.
• Aislamiento repetido en el CAE de patógenos Gram(-), P. Aeruginosa predominantemente.
Levenson(1991) y Ceruse (1993):
— Otitis externa refractaria.
— Otalgia severa, que empeora a la noche.
— Exudado purulento.
— Tejido de granulación.
— Aislamiento de Pseudomona.
— Tc 99 (+) de hueso temporal.
— Diabetes Mellitus u otras patologías inmunocompetentes.
Imágenes
— Radiografía estándar: Aunque la radiografía estándar es más económica y accesible; no aporta datos específicos ni significativos para el diagnóstico de OEM.
— Tomografía computada (TAC): Este examen es indudablemente mas útil para determinar erosiones óseas y compromiso de partes blandas, tales como articulación temporomandibular, mastoides, peñasco, otros sectores de la base del cráneo, tejidos blandos, endocráneo, etc. Además, puede revelar cambios inflamatorios en la cavidad timpánica, mastoidea, fosa infratemporal, espacio parafaríngeo y nasofaríngeo; así como el área del agujero estilomastoideo, donde se compromete con mayor frecuencia el nervio facial.
La relevancia diagnóstica de este método, esta principalmente representado por la capacidad de evidenciar la extensión de las erosiones óseas.
Sin embargo, la TAC no es muy útil cuando comienza el compromiso óseo; cuando la erosión del hueso trabecular es menor del 30 a 50%.
Además, cuando el área de osteomielitis ya ha sido determinada o revelada por una TAC anterior, la imagen diagnóstica raramente revierte a la normalidad.
Es por ésta razón que la TAC es de pequeño valor para determinar la respuesta terapéutica.
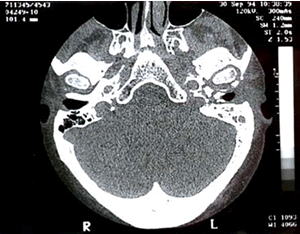
7 – TAC óptico del oído izquierdo en el que se observa una lisis de la pared anterior del CAE con secuestros óseos correspondientes a una otitis externa maligna.
— Resonancia magnética nuclear (RMN): La RMN con Gadolinio ha demostrado ser superior que las demás técnicas por imágenes para evaluar las complicaciones de los tejidos blandos intracraneales. Esta provee imágenes detalladas y seguras de la extensión de la enfermedad, revelando cualquier complicación de los forámenes basales y en consecuencia de los nervios craneales así como de las meninges. Es el mejor método para el estudio de la articulación temporomandibular y del CAE óseo y membranoso.
No obstante así como con la TAC, las imágenes patológicas que se evidencian con RMN permanecen inalteradas por un largo tiempo después de la regresión de la enfermedad. Por lo tanto ésta técnica es de poco uso para evaluar los efectos terapéuticos.
— Centellografía con tecnecio 99 y Galio 67: Estas dos técnicas proveen imágenes muy importantes en los diferentes estadios de la enfermedad.
— A. Tecnecio 99 Esta sustancia es depositada en el hueso; pero permanece incierto si ésta es depositada dentro de la hidroxiapatita en estadio de cristales o la inversa al inicio del proceso de hidrólisis. Tc99 indica actividad osteoblástica inespecífica ya que puede ser encontrada en áreas de osteomielitis aguda o crónica del peñasco o de la base del cráneo; así como en procesos no infecciosos como neoplasias primarias o secundarias.
Aunque el Tc 99 ofrece solo una modesta resolución espacial, no permite una buena discriminación de las partes anatómicas comprometidas. De éste modo se puede comprobar que el método es relativamente inespecífico y la información ha de ser interpretada desde el punto de vista de su contexto clínico, esto tanto como para el diagnóstico como para la evolución de la enfermedad. En efecto, el defecto de la técnica es que igual, después de la regresión de la enfermedad los registros óseos permanecen positivos por una cantidad de tiempo variable (9 meses a varios años), como consecuencia de la formación y remodelación de hueso nuevo.
Como resultado de esto, los registros con Tc 99 son de poco valor para el seguimiento de los pacientes afectados con OEM, y sobretodo en decisión de cuando interrumpir el tratamiento antibiótico.
Finalmente, hay que recordar que también se observa un leve incremento en la captación del radionucleótido en pacientes en pacientes con otitis externa severa, pero no maligna.
De cualquier modo la diferencia en cuanto a cantidad de captación entre el lado enfermo y el contra lateral (registro cuantitativo) permite una fácil distinción entre las dos formas ya que la diferencia es mucha mayor en los casos de OEM.
— B. Centellografía con Galio 67: Esta es una técnica de gran utilidad; la cual es complementaria al Tc 99 en muchos aspectos en los registros óseos. El Citrato de Ga 67 es presumiblemente incorporado dentro de las proteínas y leucocitos que se acumulan en los sitios de actividad inflamatoria como complejo Ga 67-lactoferrina. Por esta razón los registros con Ga 67 tomados aisladamente son también exámenes complementarios inespecíficos, lo cual puede resultar positivo en caso de algún proceso inflamatorio activo del oído, incluyendo una simple otitis externa en el 95% de los pacientes afectados con OEM puede ser observado un rápido incremento de la captación del radionucleótido como expresión generalizada del proceso inflamatorio, pero los registros con Ga 67 no son capaces de indicar si el proceso inflamatorio proviene de un área confinada a las partes blandas ó involucra el hueso. De éste modo la información proveniente de esta ha de ser interpretada en el contexto de un registro óseo con Tc 99; de esta forma algunas áreas de osteomielitis activa (correspondiente a un aumento de la captación de ambas, Tc 99 y Ga 67) Pueden ser distinguidas de aquellas de osteomielitis inactiva, donde solo se observa un incremento de la captación de Tc 99.
Por lo tanto:
— Osteomielitis activa: captación de Tc 99 y Ga 67.
— Osteomielitis inactiva: captación solamente de Tc 99.
Al igual que el Tc 99, el Ga 67 proporciona una pequeña resolución espacial. A
pesar de este defecto, los registros con Ga 67 son extremadamente útiles para monitorear la respuesta terapéutica. La cantidad de galio refleja el nivel de actividad de la enfermedad, y en general los registros retornan rápidamente a la negatividad al finalizar el proceso inflamatorio, aunque se han reportado casos de resolución de la enfermedad
tiempo después de completarse la desaparición de la captación de galio.
Benecke: Basados únicamente en la Centellografía:
| Estadios | Ga 67 | Tc 99 | Extensión de la Enfermedad |
| I | + | – | OEM Afección de Tejidos Blandos |
| II | + | + | Osteomielitis de la Base de Cráneo |
| III | + | + | Osteomielitis Extensiva de la Base de Cráneo |
Centellografía con Leucocitos marcados con Indium 111: Esta técnica ha sido propuesta como un método alternativo, pero no se usa corrientemente como primer método diagnóstico. Esta consiste en retornar al paciente los leucocitos radiomarcados a la corriente sanguínea; y requiere la habilidad técnica de marcarlos, y en la adquisición y selección de las imágenes. Por lo tanto la técnica requiere la incubación extracorpórea de los leucocitos con radionucleótidos, y esto acarrea el riesgo de transmisión de sangre con carga patógena, reportándose casos en la literatura de transmisión de HIV por la administración equivocada de productos sanguíneos.
Aparentemente esta técnica tiene algunas ventajas sobre el Ga 67 en el diagnóstico de la osteomielitis, y su principal fuerza ha sido que ella puede ofrecer ventajas en el establecimiento de la resolución de la infección. En contraste con el Tc 99 y el Ga 67; éste registro da hallazgos normales dentro de semanas o meses de resuelta la infección.
Entre estas ventajas tenemos:
— En particular la baja captación en la saliva, lágrimas y glándulas salivales; lo que disminuye el enmascaramiento de la captación temporal.
— El paciente recibe menos irradiación.
— No se acumulan tanto radionucleótidos en el sitio de modificaciones óseas como el Ga 67.
Basada en los mismos principios clásicos de los registros con radionucleótidos, produce una serie de cortes axiales, coronales y sagitales. Esta técnica es mas avanzada y provee detalles anatómicos mas definido y completos. Sin embargo, el In 111 puede dar hallazgos normales en casos de persistencia de enfermedad según algunos casos reportados. Además, la literatura en medicina nuclear demostró que el In 111 es particularmente poco confiable en las imágenes de osteomielitis crónica.
Se cree que la duración de la infección quizá sea un factor de taza en los falsos negativos, es así como las infecciones de mas de 2 a 3 semanas son más aptas de producir falsos negativos. La localización de la infección puede ser también un factor, por ejemplo, es alto el porcentaje (83%) de falsos negativos reportados en el diagnóstico de osteomielitis de columna vertebral. Los abscesos son otros procesos infecciosos que son diagnosticados con escasa confiabilidad por el In 111. La inmunodeficiencia también ha sido reportada como algún estorbo en la eficiencia del mismo.
La confiabilidad del centellograma con In 111 para monitorear la evolución de la enfermedad, ha sido también muy cuestionada; ya que la reducción de los límites de captación puede ocurrir en complicaciones osteomieliticas de la médula ósea; ésta reducción de las áreas frías puede llevar a la interpretación errónea de que el proceso infeccioso está mejorando. Siendo así que la presencia de secuestro y necrosis pueden albergar bacterias, y no permiten el flujo sanguíneo en la región, reduciendo el flujo y acumulo de leucocitos y la función de los mismos, implicando una infección crónica. La microangiopatía diabética puede también disminuir el flujo sanguíneo. Por último puede ser difícil la contribución de las imágenes por ellas mismas en la presencia de otros signos que asemejen una complicación de partes blandas.
Para concluir podemos decir que el In 111 es un novedoso método de estudio, el cual al igual que otros métodos de evaluación pueden dar falsos negativos; es así como sea reportado como método no seguro en el diagnóstico de la osteomielitis crónica, particularmente de la columna vertebral.
Diagnostico diferencial
Debe hacerse principalmente con NEOPLASIAS del CAE (carcinoma espinocelular).
También debe tenerse presente Granulomatosis de Wegener (Esta es una vasculitis necrotizante con compromiso preferentemente del tracto respiratorio. Se observa generalmente en pacientes de 40 años y es raro en la raza negra) e Histiocitosis (La Histiocitosis X, se refiere a un grupo de desordenes del sistema retículo endotelial que se caracteriza por una proliferación de histiocitos histológicamente benignos)
A continuación se expone un sencillo cuadro donde se explican las diferencias más importantes entre patologías del oído externo:
| Patología | Otoscopía | Secreción | Síntomas | Tratamiento |
| Otitis Externa Aguda Bacteriana | Dolorosa. Inflamación y Edema de CAE | otorrea serosa o seropurulenta | Fiebre, dolor en trago a la presión, adenitis regional | Activo frente a P. aeruginosa. Tópicos: asociación de polimixina, neomicina, hidrocortisona, Ac. cétiico 2% o de Ciprofloxacino. En casos severeos vía oral o parenteral (Ciprofloxacino, Trobamicina) |
| Otitis Aguda Externa Circunscrita (Forúnculo) | Muy dolorosa. Lesión prominente, congestiva y contenido purulento (punto blanquecino) | Inflamación dolorosa a nivel folículos pilosebáceos. Linfadenitis Regional. Dolor en trago o tracción pabellón | Habitualmente por S. Aureus. Color seco Local. Sistémicos: a) Cloxacilina 600 mg/6h b) Amoxi/Clavulánico 500 mg/8h Locales: Ciprofloxacino, Gentamicina, Neomicina. Aines. Si dolor intenso o inflamación importante: drenaje quirúrgico. |
|
| Otitis Externa Maligna (Infección grave, a veces mortal) | Tejido de granulación unión ósteo-cartilaginosa de CAE. Úlceras | Secreciones ocres verdosas | Ancianos diabéticos o inmunodeprimidos (SIDA) Cefalea. Afectación N facial. IX, X, XI si evoluciona. Menos frecuente V y VI | Pseudomona Aeruginosa. Ante sospecha reisión a especialista ORL. Iniciar tratamiento sistémico con Ciprofloxacino |
| Otomicosis (los más fracuentes son Aspergiulus, Cándidas) | CAE ocupado por una membrana grisácea con puntos negros, amarillos o blancos (hifas) | Picor intenso en la primaria. En la secundaria (superpuesta a una bacteriana): Otalgia y prurito | Limpieza repetida CAE. Aplicación Tópica de Antimicóticos. Agentes acidificantes del Medio: Alcohol boricado a saturación al 70%. Remitir a especilista ORL | |
| Miringitis Bullosa (O. Gripal) | Inflamación húmeda de color rojizo pálidocon formación de ampollas que pueden extenderse a la M. Timpánica | Aparece en el curso de un cuadro catarral. Orígien: vírico | Curación espontánea. Ibuprofenos vía oral / Tratamiento sintomático |
Tratamiento
Durante años se han hecho modificaciones sustanciales para acercarse al tratamiento adecuado para la OEM, las cirugías extensivas con extirpación de los tejidos infectados, los cuales fueron considerados originalmente el tratamiento de elección, probaron ser muy inadecuados.
Mientras tanto la introducción de antibióticos con actividad contra Pseudomona, abrieron una perspectiva para mejorar la terapéutica. Actualmente existe un acuerdo unánime que, un adecuado y suficientemente prolongado tratamiento con antibióticos, representa el pilar mayor del tratamiento de la OEM. La posibilidad de la intervención quirúrgica es reservada en forma corriente para unos pocos casos seleccionados.
Una vez hecho el diagnóstico el paciente debe ser internado; luego el tratamiento puede ser dividido en:
Tratamiento Local:
— Limpieza.
— Aspiración.
— desbridamiento.
— Gotas óticas con ciprofloxacina. Aunque el uso de agentes antimicrobianos en forma tópica es algo controversial, dado que los antibióticos administrados dentro del conducto auditivo externo producirían una variación de la flora bacteriana.
Este tratamiento local debe realizarse en forma diaria bajo control otomicroscópico, liberando el CAE de granulaciones, tejido necrótico y secuestros óseos, pudiéndose utilizar la crioterapia para el tratamiento de las granulaciones.
La acidificación del medio, con ácido bórico y jugo de limón, en forma diaria, brindan excelentes resultados en la mayoría de los casos.
Tratamiento antibiótico:
El mayor problema actualmente radica en la elección de los antibióticos y la duración del tratamiento.
1) Elección del antibiótico.
Tiempo atrás, a fines de la década de los 70 se utilizaba la asociación de aminoglucósidos y penicilinas semisintéticas (Azlocilina, Carbenicilina, Ticarcilina, Mezlocilina, Piperacilina), ya que la combinación de ambas es sinérgica contra Pseudomonas.
Esta asociación amplifica el espectro de acción y reduce la posibilidad de resistencia. De todos modos el empleo de aminoglucósidos (entre ellas la Tobramicina, la cual es más efectiva que la Gentamicina, está relacionada con una mayor proporción de efectos adversos, principalmente enlazada con su bien conocida oto y nefrotoxicidad.
En adición a esto, con la OEM estos antibióticos deben ser administrados durante periodos muy largos, esto lleva a un alto riesgo y la necesidad de someter al paciente a chequeos frecuentes de función renal, de función cócleo-vestibular y de los niveles de droga en sangre. El empleo también de penicilinas semisintéticas, las cuales son bactericidas, es potencialmente asociado con efectos adversos, tales como retensión de sodio, depleción de potasio, hipertransaminasemia, sangrado espontáneo, anemia hemolítica y convulsiones; a su vez ésta, debe estar asociada con un cuidadoso monitoreo cardiológico y hematológico, con una dieta hiposódica.
Durante la década de los 80, se utilizaron cefalosporinas de tercera generación, las que se establecieron por ser activas contra Pseudomona y ser efectivas en el tratamiento de la osteomielitis. Ello comenzó a dar una plaza en el tratamiento de la OEM, en particular la Ceftazidima; B-lactamasa resistente, bactericida para Pseudomona y otros gérmenes Gram (-). Con una dosis de 2gr c/8 hs, ha sido efectiva en controlar muchos casos de OEM cuando son administradas solas o en asociación con Tobramicina. Sin embargo, esta forma de tratamiento, tiene sus desventajas en el sentido de que requiere administración endovenosa por periodos prolongados de tiempo y así aumentan tanto los cuidados como los costos hospitalarios.
Actualmente se usa la Ciprofloxacina, la cual es una Fluoroquinolona. Estas son activas contra Pseudomona y se pueden utilizar por vía oral, sola o en combinación con otros antibióticos para el tratamiento de la osteomielitis de la base del cráneo.
El mecanismo de acción puede ser atribuido a la inhibición de la subunidad A de
la ADN girasa bacteriana (enzima bacteriana involucrada en la duplicación del ADN bacteriano).
Las fluoroquinolonas cuando son administradas por vía oral, rápidamente alcanzan altas concentraciones en sangre, orina y sobretodo en los tejidos, con una eficiente penetración en hueso. Es bien absorbida en el tracto gastrointestinal, pero los pacientes deberán tener la precaución de no tomarlo con antiácidos con sales de magnesio, dado que esto produce una disminución de su absorción. Su vida media relativamente larga, le permiten intervalos de dosis más amplios en relación con otras drogas (8-12hs).
Los efectos adversos reportados con mayor frecuencia son:
— Gastrointestinales: nauseas y vómitos.
— SNC: cefaleas, alteraciones en el equilibrio.
— Piel: rash y erupciones cutáneas.
Estos efectos adversos rara vez son lo suficientemente severos como para interrumpir el tratamiento.
Dosis utilizada: 750 mg c/12 horas por vía oral durante 6 a 8 semanas.
Estas drogas pueden ser utilizadas solas o en asociación con Ceftazidima,
Penicilina semisintética o rifampicina.
Ambas drogas asociadas se han usado como terapia primaria y en él mantenimiento domestico de la terapia siguiendo al tratamiento parenteral realizado en el hospital.
En todos los casos esto lleva a muy buenos resultados; y es así como esta droga en la práctica aventaja en la administración oral, permitiendo un posible tratamiento ambulatorio, con baja toxicidad y con un costo reducido. Esto ha llevado a que algunos autores indiquen en forma entusiasmada estos antibióticos para el tratamiento de la OEM.
Algunos autores manifiestan que el tratamiento de esta patología con la asociación de beta-lactámicos y aminoglucósidos es eficiente, segura y productiva como el tratamiento con quinolonas y cefalosporinas de tercera generación, lo cual también ha sido reportado años atrás; los cuales sugieren reservar ésta combinación para tratamientos fallidos, desarrollo de resistencia o efectos colateral. Sin embargo, otros autores deciden esperar un tiempo mas prolonga para su confirmación, recomendando el empleo de las quinolonas solo después de un adecuado periodo inicial de tratamiento con aminoglucósidos más penicilinas semisintéticas, u otra en asociación con Ceftazidima.
En los casos de OEM causada por hongos algunos autores usaron con éxito la
Anfotericina B, sola o en combinación con Rifampicina.
2) Duración del tratamiento antibiótico:
Durante los últimos tiempos, fue indicado como norma llevar el tratamiento antibiótico por varias semanas (6-8 semanas), pero tiempo después se planteo la necesidad de encontrar un parámetro objetivo que pueda confirmar una recuperación completa de la enfermedad.
Algunos autores proponen un criterio basándose en la curación del proceso a
nivel de la piel del CAE y la negativizaciòn de los cultivos provenientes de la secreción del oído.
Recientemente otros autores han sugerido como parámetro mas seguro una normalización de la Eritrosedimentación.
Otros continúan usando la terapia hasta que la Centellografía con galio se normalice completamente; este último criterio ha sido sustentado como método mas seguro como para indicar el nivel de actividad de la enfermedad. No obstante debería recordarse que esta es limitada por su pobre resolución espacial y que los hallazgos por esta técnica no son por ella misma suficientes como para hacer una evaluación completa, y necesita ser interpretada en el marco de todo el contexto clínico del paciente.
— Tratamiento quirúrgico: A diferencia de las décadas anteriores, actualmente la cirugía solo cumple un rol complementario.
La cirugía puede consistir en una mastoidectomia definitiva con timpanoplastìa de ser necesaria, pero muchos autores recomiendan biopsia y limpieza del conducto, con resecciones periódicas de los tejidos necróticos, granulomas tisulares colecciones de pus y secuestros óseos y cartilaginosos.
En general excepto por secuestro óseo, algunos autores manifiestan que él tratamiento quirúrgico es impracticable en la OEM a causa de la penetración profunda en la base del cráneo y a la falta de líneas demarcatorias en este proceso tan difuso. Hoy en día es preferible un largo periodo de tratamiento antibiótico, siendo el desbridamiento del conducto auditivo externo el tratamiento quirúrgico a realizar en forma diaria hasta resolver todo tipo de granulación.
— Tratamiento adyuvante: Oxígeno terapia hiperbárica (OHB).
Medicina Hiperbárica – Bs As 10 de Enero de 2005 –
El tratamiento con oxígeno hiperbárico es un tipo de terapia no invasiva. El paciente respira tranquilamente 100 % de oxígeno mientras permanece en una cámara presurizada a una presión mayor que la presión atmosférica ambiental. Involucra la administración de oxígeno sistémico a presiones dos o tres veces superiores a la atmosférica.
Es la única terapia indicada en ciertos casos y en muchos otros ayuda en el
tratamiento de enfermedades y problemas clínicos o quirúrgicos difíciles, aparte de
producir un efecto revitalizador en todos los tejidos.
Notas Históricas sobre Medicina Hiperbárica
Datos de tratamiento hiperbárico se tienen desde 1662 con el médico británico Henshaw, mucho antes de que se identificara el oxígeno como elemento individual. Este médico intuyó que el aumento elevado de la presión del aire podría aliviar algunas lesiones graves, y la presión barométrica baja mejoraría condiciones crónicas.
Médicos europeos como Junod (1834), Pravaz (1837) pusieron hitos en terapias hiperbáricas. Los «baños con aire comprimido» se extendieron por toda Europa y atrajeron pacientes de sitios lejanos incluido Estados Unidos.
En América la primera cámara hiperbárica fue construida en Canadá, en 1860, un año después en New York, para tratamientos de desórdenes nerviosos.
Corning (1881), Cuninghan (1921), Drager (1917) tuvieron éxitos en terapias hiperbáricas.
Es en 1937 que Behnke y Shaw usaron el oxígeno hiperbárico para la enfermedad por descompresión.
Entre 1950 y 1960 se aceleró el estudio del oxígeno en los campos de la aviación y el buceo marino, especialmente por la NASA; al trascender estas investigaciones a la comunidad científica se incrementaron las aplicaciones terapéuticas.
Desde la fundación de la Undersea and Hyperbaric Medical Society (UHMS) en 1967, en muchos países se conforman organizaciones médicas dedicadas a la investigación y tratamientos con oxígeno hiperbárico. Hoy en día se tienen cámaras hiperbáricas difundidas en todo el mundo y esta terapéutica se ha convertido en una moderna especialidad.
EFECTOS BENEFICOS DE LA TERAPIA CON OXIGENO HIPERBARICO
El kid del tratamiento con oxígeno hiperbárico radica en la factibilidad que presenta el plasma sanguíneo (que es el líquido donde flotan los glóbulos rojos) de permitir la dilución del oxígeno, incrementando de diez a quince veces la concentración de este elemento, lo que produce un incremento cuatro veces mayor de difusión de oxígeno desde los capilares funcionales a las células, independientemente de que el nivel de oxígeno llevado por la hemoglobina de los glóbulos rojos permanezca igual.
Revitalización y Neovascularización
De esta manera las células lejanas a los capilares y que sufren hipoxia (bajo aporte de oxígeno) se ven revitalizadas con el oxígeno hiperbárico, pueden cumplir nuevamente sus funciones, se multiplican y piden más oxígeno por lo que se forman nuevos vasos sanguíneos (neovascularización), efecto indirecto del oxígeno hiperbárico, con lo que se revitaliza el tejido, el órgano y el paciente.
Acción Antimicrobiana
La terapia con oxígeno hiperbárico produce inhibición e inactivación de las toxinas en infecciones por Clostridium perfringes (gangrena gaseosa), a la vez que elimina bacterias anaeróbicas. Favorece la fagocitosis y la lisis oxidativa de los leucocitos. Potencia la actividad de los aminoglucósidos. Tiene un efecto postantibiótico prolongado cuando se lo combina con tobramicina para combatir la Pseudomona aeruginosa.
Efecto Vasoconstrictor y Antinflamatorio
Produce constricción vascular con lo que se evita la extravasación de líquidos desde los capilares, disminuyendo los edemas. Lo singular es que este efecto se establece sin hipoxia. Por esta razón es aplicable en las isquemias traumáticas y en el síndrome compartimental. Ayuda a reducir el edema intersticial en tejidos injertados y los mantiene oxigenados revitalizándolos, así como disminuye el tiempo de recuperación postraumática y posquirúrgica. El postoperatorio de las cirugías plásticas es totalmente garantizado con la oxigenación hiperbárica.
Efecto similar se produce en heridas por quemaduras reduciendo significativamente la cantidad de líquidos requeridos para estos pacientes que se recuperan maravillosamente.
Efecto de Presión Directa
Se fundamenta en la Ley de Boyle: a mayor presión, menor volumen de un gas, sea intravascular o libre. Así se justifica el tratamiento con oxígeno hiperbárico en la enfermedad por descompresión y embolismo gaseoso, casi siempre asociada al buceo, provocada por burbujas de nitrógeno, mismas que se verían reducidas y disueltas por la simple presurización.
Radicales Libres
La terapia con oxígeno hiperbárico aumenta los niveles de superoxidasa dismutasa (SOD), glutatión y catalasa que son antioxidantes naturales que nos protegen de los radicales libres, factores éstos que lesionan nuestras células.
La Terapia con Oxígeno Hiperbárico como Medicina Preventiva
En base de los razonamientos anteriores la oxigenación hiperbárica no sólo está indicada para los pacientes que sufren determinada enfermedad, sino que puede ser utilizada por todas las personas con el propósito de revitalizar todos sus órganos y de esta manera prevenir enfermedades, mantenerse saludables y prologar la vida con calidad. Recordemos que el oxígeno hiperbárico «es en realidad un normalizador y regulador de todas las funciones biológicas: eleva el sistema inmunológico, tonifica la piel, previene o corrige la hipoxia que, en general, es el factor subyacente de casi todas las dolencias».
RESUMEN DE INDICACIONES INTERNACIONALES (Jain)
— Enfermedad por descompresión.
— Embolismo aéreo.
— Envenenamiento: monóxido de carbono, cianuro, ácido sulfhídrico, tetracloruro de carbono.
— Tratamiento de ciertas infecciones, gangrena gaseosa, fasceítis necrosante aguda, micosis refractaria, lepra, osteomielitis.
— Cirugía plástica y/o reconstructiva. Heridas no cicatrizables. Ayuda para la cirugía de reimplantación. Ayuda para la supervivencia de colgajos con circulación marginal. Apoyo para el tratamiento de quemaduras.
— Traumatología: heridas por aplastamiento, síndrome compartimental, lesiones deportivas de tejidos blandos.
— Ortopedia: fracturas no consolidadas, injertos óseos, osteorradionecrosis.
— Vasculopatías centrales: shock, isquemia miocárdica, ayuda para la cirugía cardiaca.
El principio fundamental de la oxigenoterapia hiperbárica, es incrementar la cuota de oxígeno disuelto en el plasma y permitir su difusión por los fluidos y tejidos según los coeficientes de solubilidad de los mismos, en cantidad inversamente proporcional a la distancia de las áreas perfundidas. Entre las indicaciones corrientes figuran la Osteomielitis aguda y crónica y la necrosis de los tejidos blandos.
Este tratamiento consiste en colocar al paciente en una cámara hiperbárica a 2 Atmósferas una hora y media por día durante 30 días.
EFECTOS NOCIVOS DE LA TERAPIA CON OXÍGENO HIPERBÁRICO
Sin embargo, la oxigenoterapia no ha sido reportada libre de riesgo como por ejemplo el barotrauma en el interior del oído, puede producir convulsiones por O2, especialmente si el tratamiento se realiza a presiones mayores de 2,4 atmósferas absolutas (ATA), puede aparecer toxicidad pulmonar por O2, que consiste en dolor torácico subesternal, tos y atelectasias. Tras 20-30 sesiones en la cámara puede aparecer entumecimiento de los dedos, especialmente de distribución cubital, sensación que desaparece a las 4-6 semanas de finalizar el tratamiento; puede producir otitis serosa, lo cual es un problema menor, que se trata con descongestivos. Uno de los efectos colaterales más frecuentes es un cambio en el poder de refracción del cristalino, la miopía en los ancianos tiende a empeorar, entre 4 y 6 semanas después del tratamiento se vuelve al estado de refracción inicial.
Una contraindicación absoluta del tratamiento con OHB es la presencia de un neumotórax no tratado, porque con la descompresión el aire intrapleural puede doblar o triplicar su volumen a medida que se acerca a la presión atmosférica normal, otra es la administración simultanea de doxorrubicina lo cual ha provocado la muerte en ratas, probablemente por cardiotoxicidad, así mismo el disulfiram bloquea la producción de superóxido dismustasa, un antioxidante protector, y también esta contraindicada su administración; de igual manera el cisplatino administrado junto con el OHB disminuye la resistencia a la tracción de las heridas en cicatrización. Los niños prematuros son susceptibles de presentar fibroplasia retrolental, por lo que en ellos el OHB está contraindicado. Los recién nacidos a término pueden tratarse con seguridad.
Entre las contraindicaciones relativas tenemos el antecedente de neumotórax espontáneo, la cirugía torácica previa, el enfisema grave con retención de CO2. Las IVRS que pueden dificultar que el paciente iguale las presiones en oídos y senos. El antecedente de una cirugía previa en el oído medio, como la otosclerosis, lo cual puede producir el desplazamiento de algún elemento de plástico al aplicar la presión si el paciente no puede igualar la presión en sus oídos, en cuyo caso puede ser necesario la utilización de tubos de timpanostomía. La existencia de trastornos convulsivos puede aumentar la susceptibilidad a presentar convulsiones por O2, por lo que es prudente realizar una premedicación adecuada (p. Ej. con diazepam). La fiebre elevada no controlada puede predisponer a la aparición de convulsiones.
Las infecciones respiratorias víricas tienden a empeorar con el OHB, y una infección de este tipo constituye un motivo para interrumpir temporalmente las sesiones diarias en los tratamientos de algunas enfermedades crónicas. En la esferocitosis congénita, los hematíes son frágiles y las elevadas presiones de O2 pueden ocasionar una hemólisis grave. Se han comprobado casos de ceguera después del tratamiento con OHB en pacientes con antecedentes de neuritis óptica, incluso sin ser ésta activa. Aunque es una situación poco frecuente, se debe interrumpir inmediatamente el tratamiento si el paciente refiere cambios súbitos en su visión. Por eso, éste método terapéutico es generalmente recurrido en los casos mas complicados de OEM siendo una terapia adyuvante de primera línea
Tratamiento de la patología de base: DIABETES.
Los pacientes con osteomielitis de la base del cráneo, frecuentemente, sufren múltiples problemas médicos como resultado de su diabetes pobremente controlada.
Algunos de estos pacientes deberían ser cuidadosamente monitoreados y tener un estricto control de sus niveles de glucemia.
Se debe realizar un monitoreo estricto de la función renal dado que los pacientes
Diabéticos están propensos a sufrir disfunciones renales, agregándose como factor de riesgo la utilización de antibióticos aminoglucósidos para el tratamiento.
CONCLUSIÓN
La otitis externa maligna, si bien es una entidad no tan frecuente, puede aparecer como una complicación de una otitis externa, principalmente en pacientes inmunosuprimidos, diabéticos y añosos, siendo excepcional en el niño, en mas del 95% de los casos el germen causante es Pseudomona aeruginosa, aunque hay reportes cuya etiología es fúngica, e incluso otras bacterias, como S. epidermidis, S aureus.
Es importante educar a estos pacientes a no manipular sus oídos y moderar el ingreso de agua en el CAE, evitando, desde el punto de vista medico, realizar lavajes quedando como única indicación aspiración de oídos.
Si no se instaura un tratamiento adecuado y oportuno, avanza indefectiblemente a una osteomielitis de base de cráneo, elevándose aun mas la mortalidad cuando existe compromiso vascular o de pares craneales (mas comúnmente afectado es el VII al salir de agujero estilomastoideo, siguiendo agujero rasgado posterior)
Se presenta casi siempre con las típicas granulaciones del CAE, los cuales se deben biopsiar para una correcta tipificación etiológica, dolor y otorrea son sumamente frecuente en esta patología, y en ocasiones, también se asocia Hipoacusia conductiva leve, manteniéndose el tímpano intacto en la mayoría de los casos.
La TAC se utiliza para diagnostico temprano, detectando compromiso óseo.
La centellografìa con Tc 99 se utiliza para detectar cualquier componente osteomielitico y el Ga 67 para monitorear la respuesta al tratamiento antibiótico (principalmente ciprofloxacina).
También en estos enfermos debe tenerse en cuenta y tratarse la diabetes, estado de inmunosupresion y aplicar un manejo local enérgico.
Debe realizarse interconsultas con otras especialidades, entre ellas endocrinólogo, clínico e infectòlogo.
Siempre tener presente que puede tratarse de una Neoplasia de CAE.
En la actualidad es una patología cada vez menos frecuente, debido al entrenamiento
medico, antibiótico terapia efectiva y métodos de diagnósticos cada vez más certeros. De todas maneras, esta entidad debe estar siempre presente en la mentalidad no solo del otorrinolaringólogo, sino que debemos incluir el medico clínico, debiendo esta ultimo actuar de manera ágil y derivando adecuadamente para su resolución.
BIBLIOGRAFÍA
Abello, Trasera: Otorrinolaringología. Doyma, 1992.
Alcides S, Kaminszcik: Otitis externa maligna. Revista de la Federación Argentina de sociedades de otorrinolaringología; Año 7-Nº1-2000.Pág 89-93.
Amorosa, Modugno, Pirodda: Malignat external otitis. Acta Otolaryngol 521 (suppl): 3-16, 1996.
Anderhuber, Walch, Kole : A rare case of malignant Otitis external in a non-diabetic patient. Laryngorhinootologie 1995 Jul;74(7):456-9.
Cerse, Mohammedi, Muller, Vautrin, Truy: Diagnostic criteria for progressive necrotizing external otitis. Are scintigraphic findings reliable?. Presse Med 1998 Jan 10;27(1):11-4.
Chai, Auret, Christiansen, Yuen, Gardam : Malignant otitis externa caused by malassezia sympodialis. Head Neck 2000 Jan; 22(1):87-9.
Cummings, Fredrickson, Harker, Krause, Richardson, Schuller: Otolaryngology-Head & Neck Surgery. Tercera edición. Vol. 4, cap. 152 , Pág : 2995-96 ; cap 157 , Pág : 3088-90.
Cunningham M.; Yu VL.; Turner J.; Curtin H: Necrotizing otitis external due to Aspergillus in an inmunocompetent patient. Archives of Otolaryngology – Head & Neck Surgery. 114(5):554-6, 1988 May.
Diamante: Otitis externa maligna. Actualización .Revista ORL Fundación de otorrinolaringología. Año 13-Nº 27. 2004. Pág.: 83 – 84.
Eleta, Velan, San Roman, Blejman, Rasumoff, Bais, García Mónaco, Secco, Durey: Diagnóstico por imágenes en medicina. Cabeza y cuello. Copyright, 1966.
Grandis JR, Curtin HD,Yu V: Necrotizing (malignant) external otitis: prospective comparison of CT and MR imaging in diagnosis and follow up. Radiology 1995 Aug; 196(2). Pág:499-504.
Paparella, Shumrick, Gluckman, Meyerhff: Otorrinolaringología. Tercera edición. Panamericana. Tomo 2 . Pag : 1325-1326.
Redleaf, Angeli, Mc Cabe: Indium 111-Labeled white blood cell scintigraphy as an unreliable indicator of malignant external otitis resolution. Ann Otol Rhino Laryngol 103, 1944. Pág.:444-447.
Robbins, Cotran, Kumar: Patología estructural y funcional. 4ta edición. Vol. 2 Pág : 785-788, año 1990.
Soldati, Mudry, Monnier : Necrotizing otitis externa caused Staphylococcus epidermidis. Eur Arch Otorhinolaryngology 1999;256(9):439-41.
Sordeli, Cerquetti, Iglesias, Catalano: Bacteriología Médica. Primera edición.Cap. 20.
Stokkel, Takes, Smit, Baatenburg de jong: The value of quantitative gallium-67 single-photon emission tomography in the clinical management of malignant external otitis. European Journal Nuclear Medicine Vol. 24, Nº11, November 1997. Pág.:1429-1432.



